Lo studio, pubblicato dalla prestigiosa rivista NAR, condotto presso il dipartimento di Drug Discovery and Development dell’IIT di Genova, ha chiarito il meccanismo d’azione di una proteina (Polimerasi-η) strettamente legata all’insorgenza del melanoma.
Il lavoro, coordinato da Marco De Vivo e portato avanti dal PhD-Fellow Vito Genna, in collaborazione con l’EPFL (École Polytechnique Fédérale de Lausanne), riporta i dettagli molecolari alla base del processo di riparazione, operato da Polimerasi-η, del DNA danneggiato dai raggi-UV e spiega come l’alterazione di questo processo sia legato l’insorgenza del tumore della pelle. Tali risultati permettono quindi di comprendere a fondo il meccanismo enzimatico di Polimerasi-η che, viste le sue funzioni, si candida a diventare un possibile target terapeutico contro il melanoma.
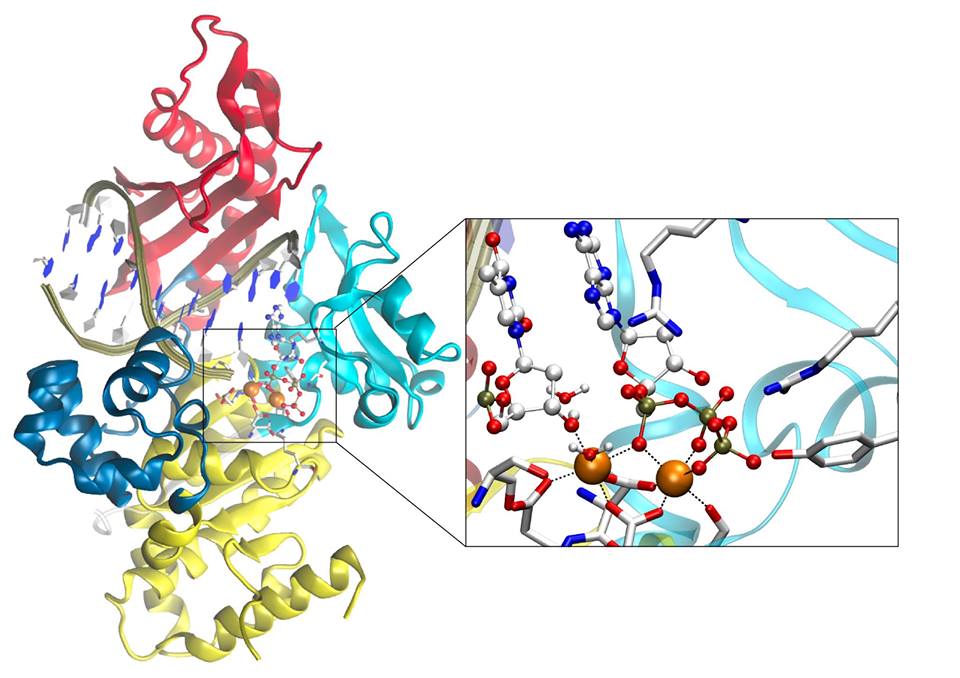
Mediante l’utilizzo di potenti super-computer gli scienziati hanno potuto simulare, atomo per atomo, le reazioni molecolari alla base del processo di riconoscimento tra Polimerasi-η e la doppia elica di DNA danneggiato. Questo ha anche permesso di comprendere nel dettaglio i moti specifici attraverso i quali Polimerasi-η modifica la propria struttura tridimensionale per riparare efficacemente la lesione presente nel DNA, un meccanismo alla base della vita.
Brevemente, all’interno di ogni cellula vivente, ogni giorno, il DNA è fedelmente replicato per garantire la corretta trasmissione dell’informazione genetica da una generazione cellulare alla successiva. Tuttavia, l’esposizione di un organismo agli stimoli ambientali, interferisce continuamente con questo processo. I raggi-UV, componente rilevante della luce solare, sono responsabili di una delle forme più diffuse di danno genetico determinato da un’insolita formazione di due legami tra due basi contigue nella doppia elica di DNA. Se questo danno si accumula in modo anomalo, la cellula può essere condotta verso la morte o, peggio, verso una deriva tumorale.
Per ovviare a questo problema la natura, nel corso dell’evoluzione, ha sviluppato degli strumenti (specifiche proteine) capaci di riconoscere selettivamente il danno lungo il filamento di DNA e ripararlo, garantendo quindi la corretta trasmissione dell’informazione genetica lungo le generazioni cellulari. Una di queste proteine, la DNA Polymerase-η, è responsabile della riparazione del materiale genetico affetto da errori indotti anche dall’esposizione ai raggi-UV. La DNA Polymerase-η ripara, però, anche il DNA di cellule tumorali danneggiate da attuali farmaci anticancro, che così sono resi inefficaci. Comprendere i meccanismi di riparazione del DNA è dunque fondamentale nel contesto delle ricerche sul cancro, come testimoniato dal premio Nobel per la Chimica 2015 per gli studi in merito di Lindhal, Modrich e Sancar.
I risultati di questo studio aiuteranno, nell’immediato futuro, la progettazione di un nuovo farmaco antitumorale altamente selettivo in grado di inibire, e quindi spegnere, l’elevata attività della Polimerasi-η all’interno delle cellule tumorali.
JOURNAL: Nucleic Acids Research
TITOLO DELLO STUDIO: Cooperative motion of a key positively charged residue and metal ions for DNA replication catalyzed by human DNA Polymerase-η
AUTORI: Vito Genna, Roberto Gaspari, Matteo Dal Peraro, Marco De Vivo
COVER: DNA Polymerase-η (Pol-η) bypasses UV-induced DNA damages via a two-metal-ion mechanism that assures DNA strand elongation and correct genetic inheritance to the new cells generation. Two identical ternary complexes formed by Pol-η, double strand DNA and the incoming nucleotide, are shown. The coordination to the key two metal ions, in the active site, is displayed in the protein on the front. The complex in the back suggests a DNA-damage caused by UV light. Original cover image by Vito Genna. The authors wish to thank Valentino Genna for his kind contribution to graphic design. For more information see article by Genna, V. et al., pages 2827–2836 in this issue.
LINK AL PAPER: http://nar.oxfordjournals.org/content/early/2016/03/01/nar.gkw128.full?keytype=ref&ijkey=nJMx86puyXaYRKk
LINK AL VIDEO: https://www.youtube.com/watch?v=8MidZstfyOU&feature=youtu.be